Карбонові кислоти — просто про складне
Коли щось пахне оцтом — згадується дитинство. Баночка маринованих огірків, крапля лимонного соку на пальці чи апельсин у чаї — все це має спільний хімічний корінь. Ім’я йому — карбонова кислота. Але не поспішайте уявляти підручник. Сьогодні поговоримо про них по-людськи — без формул, але з реальними прикладами.
Що таке карбонові кислоти — і чому вони поруч з нами
Уявіть собі, що хімія — це кухня. І карбонові кислоти — це спеції, які змінюють смак усього. Вони входять до складу оцту, фруктів, жирів і навіть мазей, якими ви лікуєте опіки. Їхня головна фішка — особлива група атомів, яка дає кислий смак.
Це не щось екзотичне. Якщо ви колись нюхали мурашину кислоту (так, її справді добували з мурах), або натиралися кремом із саліциловою — ви вже знайомі з ними. Ці речовини оточують нас у їжі, медицині, косметиці та навіть у біології нашого тіла.
Придивіться до складу звичайного продукту на полиці — і, ймовірно, знайдете там щось «-ова кислота».
 Класифікація: від простих до складних
Класифікація: від простих до складних
Як і в будь-якому гурті, у світі карбонових кислот є свої типажі. Ось кілька прикладів, які можна запам’ятати без зайвої науки:
Оцтова кислота — для маринаду
Мурашина — для захисту тварин
Лимонна — в улюблених цукерках
Саліцилова — проти прищів
Стеаринова — у милі
І це тільки початок. Їх класифікують за кількістю кислотних груп, за будовою ланцюга та навіть за тим, де вони трапляються в природі. Але замість теорії — приклад: лимонна кислота — це трьохосновна, бо має три «кислих хвостика». Саме тому вона така активна.
Якщо вам треба щось видалити з поверхні — шукайте саме багатоосновні кислоти. Вони найдієвіші.
Їхні властивості — не лише смак
Карбонові кислоти можуть здивувати. Наприклад, самі по собі вони не страшні — але в певних умовах можуть роз’їдати метал. Багато з них добре розчиняються у воді. Деякі — летючі та мають виразний запах (згадайте оцет).
З іншого боку, є такі, що схожі на віск — тверді, майже без запаху, жирні на дотик. Тому з них роблять мило, креми, пластмаси. Їх поведінку визначає структура: чим довший ланцюг — тим менш летка й більш жирна кислота.
Якщо ви відчуваєте щось різке на запах — цілком можливо, що це летка карбонова кислота.
Як їх отримують — у лабораторії й у природі
У природі все геніально. Мурахи самі виділяють кислоту для захисту. Плоди накопичують її для смаку. А от у лабораторії все цікавіше: можна взяти спирт, нагріти, додати кисень — і отримаєш кислоту. Так, хіміки — теж трохи кулінари.
З побутових прикладів — оцтова кислота утворюється з вина, яке “закисло”. Тобто, просто додайте повітря — і отримаєте щось зовсім інше.
Цікаво: саме так колись готували оцет у монастирях — без реактивів, просто на відкритому повітрі.
Застосування — від борщу до ліків
Це, мабуть, найцікавіше. Карбонові кислоти — не лише в пробірках. Вони — в нашому домі.
Харчова промисловість: оцтова (маринади), лимонна (цукерки, газовані напої)
Косметика: саліцилова (креми, маски, шампуні)
Фармацевтика: ацетилсаліцилова (аспірин)
Побут: стеаринова (мило, свічки)
І навіть в організмі — вони частина обміну речовин, забезпечують енергію клітинам. Без них життя було б прісним — у прямому й переносному сенсі.
Наступного разу, коли мазатимете крем — згадайте, що він має хімію, яка з вами з дитинства.
 Кислоти, які ви точно знаєте (хоч і не підозрювали)
Кислоти, які ви точно знаєте (хоч і не підозрювали)
Давайте зберемо знайомі назви в один ряд:
| Назва | Де зустрічається | Що робить |
|---|---|---|
| Оцтова | Маринади, приправи | Додає кислоту, зберігає |
| Мурашина | Укус мурах, консервант | Захищає, знежирює |
| Лимонна | Фрукти, напої | Дає кислинку, зберігає |
| Саліцилова | Косметика, ліки | Протизапальна дія |
| Стеаринова | Мило, креми, свічки | Дає твердість, емульгує |
Тепер, читаючи склад на етикетці, ви знатимете — це не страшно, це просто хімія в дії.
Ми щодня взаємодіємо з карбоновими кислотами — навіть цього не помічаючи. Вони — не щось складне. Це те, що пахне свіжістю в салаті, лікує ранку чи тримає форму свічки. Якщо знати, як вони працюють — можна краще зрозуміти і світ, і себе.
Знання не завжди в підручниках. Іноді воно — в ложці борщу.

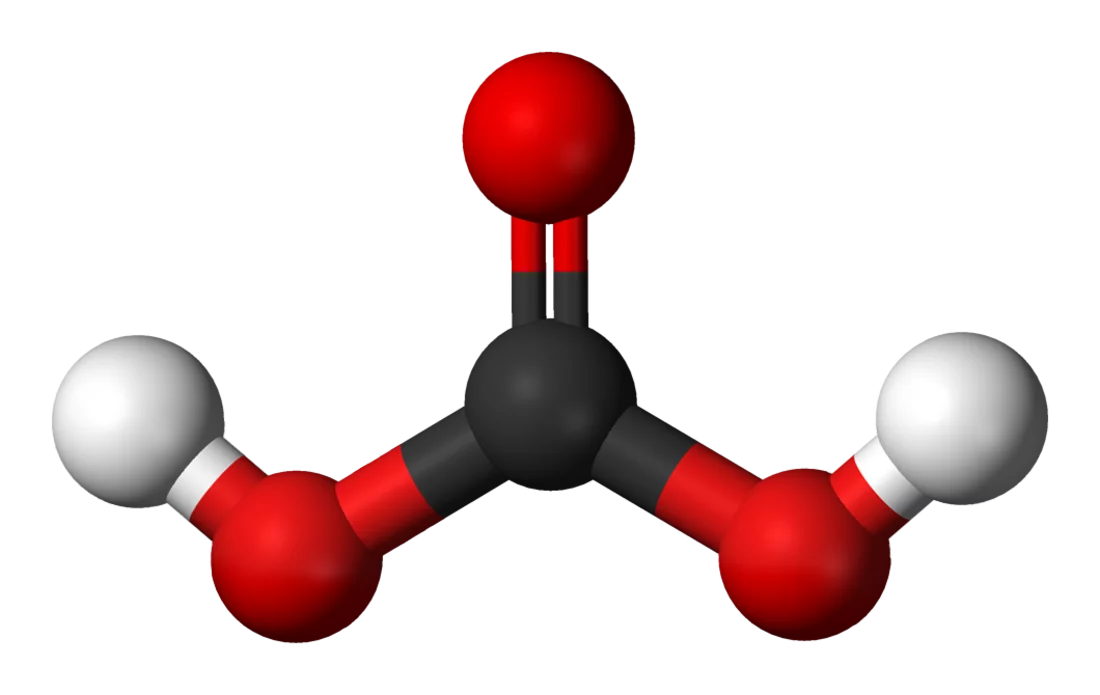 Класифікація: від простих до складних
Класифікація: від простих до складних